内容提纲:
一、什么是染色体外环状DNA
二、染色体外环状DNA在肿瘤中的功能作用
1.促进癌基因扩增
2.促进肿瘤异质性和耐药性
3.促进癌细胞基因重组
4.作为潜在分子标志物
三、云序生物提供的环状DNA研究服务
1.组织细胞环状DNA测序
2.血清血浆环状DNA测序
3.血清血浆环状DNA甲基化测序
4.环状DNAsanger测序
5.环状DNA纯化柱
1.促进癌基因扩增
2.促进肿瘤异质性和耐药性
3.促进癌细胞基因重组
4.作为潜在分子标志物
下面我们一起来看看这4方面的研究结果。
文章1:染色体外环状DNA促进染色质的开放和促癌基因的表达

发表期刊:Nature
影响因子:42.778
发表时间:2019.11.20
文章链接:Circular ecDNA promotes accessible chromatin and high oncogene expression
本文研究了三种人类癌细胞系和来自于TCGA的临床肿瘤样品,超高分辨率共聚焦显微镜展示了染色体外环状DNA游离于染色体外及它们的环状结构,并将WGS测序数据与RNA-seq数据联合,通过单核苷酸多态性分析,发现染色体外环状DNA是癌基因中表达丰度最高的基因之一。研究发现在eccDNA上面染色质的结构是高度开放的,利于基因表达,同时染色体外环状DNA的环状结构导致原本相距很远的DN**段,会被连接到一起,从而能够实现超远距离的相互作用和基因调控。本研究为深入了解染色体外环状DNA结构如何影响癌基因提供了线索,并将染色体外环状DNA与癌基因组学和表观遗传学联系起来。
文章2:环状染色体外DNA对癌基因的扩增

发表期刊:Cell
影响因子:38.637
发表时间:2019.12.12
文章链接:Functional Enhancers Shape Extrachromosomal Oncogene Amplifications
本研究发现,致癌基因EGFR基因经常会从染色体脱落而产生染色体外环状DNA,并且EGFR和其在染色体外环状DNA上序列上游非编码区的增强子在胶质母细胞瘤中共同扩增。对多种癌种的样本进行同样分析发现不同实体肿瘤类型中均存在类似的癌基因与增强子显著共扩增的现象。进一步研究证明肿瘤细胞中的癌基因通过高级扩增与环化而形成的对自身调控活性的增强,是一个十分有效的促癌机制。本文揭示了染色体外环状DNA特殊的染色质结构及其功能,为后续的基础与应用研究,奠定了重要的基础。
文章3:ecDNA与致癌基因扩增及多种癌症不良预后相关

发表期刊:Nature Genetics
影响因子:27.603
发表时间:2020.08.17
文章链接:Extrachromosomal DNA is associated with oncogene amplification and poor outcome across multiple cancers
染色体外DNA (ecDNA)扩增促进肿瘤内遗传异质性并加速肿瘤进化;然而,其频率和临床影响尚不清楚。通过对3212名癌症患者全基因组测序数据的计算分析,本文发现ecDNA扩增经常发生在大多数癌症类型中,但不发生在血液或正常组织中。癌基因在扩增的细胞外基质上高度富集,最常见的复发性癌基因扩增发生在细胞外基质上。与拷贝数匹配的线性DNA相比,ecDNA扩增导致更高水平的癌基因转录,同时染色质可及性增强,更经常地导致转录物融合。即使在控制组织类型的情况下,癌症携带内皮祖细胞基因的患者的生存期也明显短于癌症不受基于内皮祖细胞基因的癌基因扩增驱动的患者。本文的结果表明,基于ecDNA的癌基因扩增在癌症中很常见,不同于染色体扩增,导致许多癌症类型的患者预后不良。
文章4:调控癌基因转录

发表期刊:Cancer Cell
影响因子:26.602
发表时间:2021.4.8
文章链接:Oncogenic extrachromosomal DNA functions as mobile enhancers to globally amplify chromosomal transcription
本文发现,培养的胶质母细胞瘤患者来源的神经球和前列腺癌细胞中,ecDNAs具有广泛的ecDNA-ecDNA间和ecDNA-染色体间互作。ecDNA-染色体互作位点具有广泛、高水平的H3K27ac信号,主要集中在表达水平增加的染色体基因上。在前列腺癌细胞中加入含有特征增强子的合成ecDNA,导致染色体基因转录的全基因组激活。对ecDNAs的染色体靶点进行单分子分辨率的解析,发现活跃性表达的癌基因在空间上聚集在ecDNA介导的互作网络中。研究表明ecDNAs可以作为移动的转录增强子来促进肿瘤的进展,并显示了一种潜在的合成非整倍体的转录调控机制。
文章1:ecDNA促进肿瘤细胞进化和基因异质性

发表期刊:Nature
影响因子:42.778
发表时间:2017.3.2
文章链接:Extrachromosomal oncogene amplification drives tumour evolution and genetic heterogeneity
本文由加州大学圣地亚哥分校的Paul Mischel教授领导的研究团队完成,共分析了17种不同的癌细胞的ecDNA。研究发现人类近一半肿瘤存在ecDNA,ecDNA是肿瘤的关键特征,它可以编码多种促进肿瘤发生发展的基因。此外,他们还发现ecDNA上带有的原癌基因可以使肿瘤细胞对环境具有更强的适应性,位于ecDNA上或染色体内部的原癌基因拷贝机制有很大差异,以至于导致原癌基因拷贝数差异和肿瘤异质性差异。这些特性使ecDNA在肿瘤细胞发生、产生多样性及耐药性过程中发挥的作用远远大于位于染色体中的相同基因发挥的作用,即ecDNA能够驱动肿瘤的异质性和耐药性。
文章2:促进胶质母细胞瘤中耐药性作用

发表期刊:Science
影响因子:41.845
发表时间:2014.1.3
文章链接:Targeted therapy resistance mediated by dynamic regulation of extrachromosomal mutant EGFR DNA
本文在基因层面分析了胶质母细胞瘤的耐药机制,发现ecDNA通过使肿瘤迅速改变其所含癌基因的数量,在某些脑癌耐药性中发挥着核心作用,而且还能决定一个细胞是否会转变为癌细胞。EGFR TKI处理后ecDNA上的EGFR基因被去除,停药后,ecDNA上的克隆EGFR突变会再次出现,通过该途径,癌细胞可以逃避针对维持在ecDNA上的癌基因的靶向治疗。本研究揭示了ecDNA可能通过一种高度特异性、动态性和适应性的途径帮助癌细胞逃避针对ecDNA上癌基因的药物治疗,暗示了与持续给药相比,高剂量脉冲间歇治疗可能会有更好的靶向抑制作用,同时使肿瘤恢复药物敏感性。
文章3:促进神经母细胞瘤的进化

发表期刊:Nature Genetics
影响因子:27.603
发表时间:2018.5
文章链接:Discordant inheritance of chromosomal and extrachromosomal DNA elements contributes to dynamic disease evolution in glioblastoma
为了了解胶质母细胞瘤(GBM)的基因组异质性是如何导致治疗反应不良的,本研究对GBM样本、神经球和原位异种移植模型进行了DNA和RNA测序。数据分析显示,ecDNA上单核苷酸变异、局部DNA改变和癌基因扩增是从肿瘤样品传播到模型系统上的主要体细胞驱动变异。作者推断,后代细胞对ecDNA的遗传是不均匀的,而这一特征会影响后代细胞的致癌潜能。分析发现,带有癌基因的ecDNA在整个疾病过程中经常被保留。这些结果表明,染色体外的元素能使GBM进化过程中基因组异质性迅速增加,而与染色体DNA改变无关。
文章1:驱动神经母细胞瘤致癌基因组重塑

发表期刊:Nature Genetics
影响因子:27.603
发表时间:2019.12.16
文章链接:Extrachromosomal circular DNA drives oncogenic genome remodeling in neuroblastoma
本文章检测神经母细胞瘤中eccDNA,绘制了表达谱,不仅发现了多种未被发现过的eccDNA,还发现eccDNA是体细胞基因组重排的主要来源。研究揭示了eccDNA通过嵌合环化和重新整合到线性基因组中的方式,导致致癌基因重组。这种环状上产生的基因重组具有重要功能和临床意义,如果这些发现能扩展到其他癌症并更深入地进行一些分析,将为理解癌症基因重塑提供新的方向。
文章1:母体血浆中eccDNA的鉴定

发表期刊:PNAS
影响因子:9.412
发表时间:2020.1.3
文章链接:Identification and characterization of extrachromosomal circular DNA in maternal plasma
文章检测了怀孕母体血浆中的eccDNA,发现这些eccDNA分子长度呈双峰分布,eccDNA整体长度要大于线性DNA,且母体来源的eccDNA长度大于胎儿来源的eccDNA。文中提出,eccDNA的环状结构可能使他们更加耐受限制性外切酶,因此比线性DNA更加稳定。这一特性使eccDNA存在作为分子标志物的潜力。
文章2:母体血浆中eccDNA甲基化的鉴定

发表期刊:Clinical Chemistry
影响因子:7.292
发表日期:2021.2
文章链接:Characteristics of Fetal Extrachromosomal Circular DNA in Maternal Plasma: Methylation Status and Clearance
首次揭示了eccDNA的甲基化状态。研究比较了母体和胎儿来源的血浆eccDNA的甲基化密度,以及小分子和大分子之间的甲基化密度,并研究了胎儿eccDNA在母体循环中的清除情况。
我们可以看到eccDNA对肿瘤的发生发展在如此多方面具有潜在影响,无论是作为癌基因表达调控因子,还是新型的特异性肿瘤标志物,eccDNA都具有极高的研究价值,近年来已成为生物医学界火热的明星分子。那么想要揭示eccDNA的种类、表达以及功能该从何入手呢?
云序生物2019年全国首fa组织细胞环状DNA测序服务,基于circle-seq方法,通过柱纯化去除基因组DNA、酶消化去除线性DNA和线粒体DNA、滚环扩增放大信号,高效纯化富集环状DNA,具有检出率高、准确性好等优点。2020年云序生物又首fa推出血清血浆环状DNA测序服务,参考卢煜明教授团队开发的方法,充分利用Tn5转座酶高效低损地片段化环状DNA,实现血液循环系统中微量的环状DNA的检测。今年,云序生物再次全国首fa环状DNA甲基化测序服务,用酶转化法将未甲基化的C转化为U,可同时检测样品中环状DNA及其甲基化状况。另外针对测序结果筛选出的环状DNA,云序生物还提供sanger测序验证服务。
1.组织细胞环状DNA测序
2.血清血浆环状DNA测序
3.血清血浆环状DNA甲基化测序
4.环状DNA sanger测序
5.环状DNA纯化柱
1.组织细胞环状DNA测序
云序生物基于circle-seq的方法,采用多种手段包括柱纯化去除基因组DNA、酶消化去除线性DNA和线粒体DNA、滚环扩增放大信号,高效地纯化和富集环状DNA,再利用NGS测序和生信分析识别环状DNA。结合优化的实验流程,本环状DNA测序服务具有检出率高﹑准确性好等优点。
参考文献:
Circular DNA elements of chromosomal origin are common in healthy human somatic tissue
实验流程:
1)柱纯化
相对于大量存在的基因组DNA,环状DNA在细胞中的含量非常少,因此从样品中提取总DNA后,第一步需要通过柱纯化去除基因组DNA,以免测序中基因组DNA占据大部分数据量。柱纯化这一步骤十分关键,既要最大限度地去除基因组DNA, 又需最大限度保留环状DNA分子,尤其是避免丢失掉超长和超短的环状DNA。云序生物采用A&A Biotechnology的纯化柱,是绝大部分eccDNA高分文章中所使用的纯化柱,并且云序生物是该品牌在国内的唯yi总代理。

在最终测序结果证实检测到的环状DNA短至100多bp,长至9M。
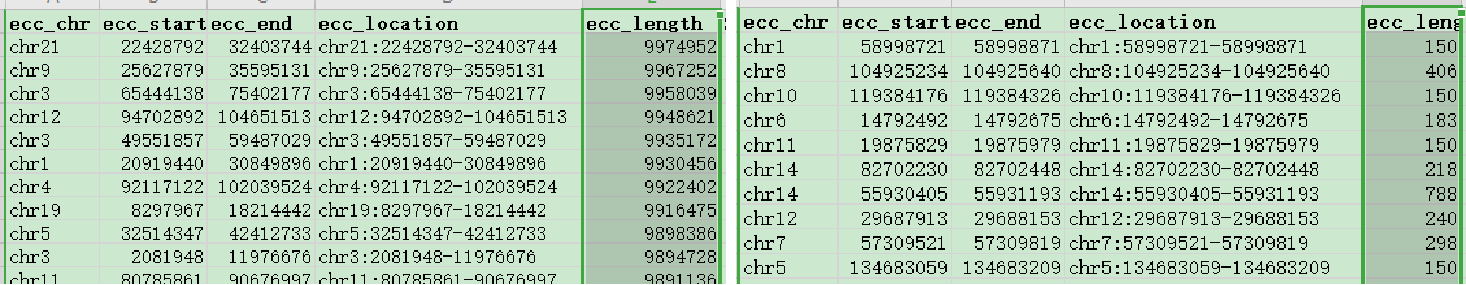
2)酶消化
经过了柱纯化,依然会有少量的线性DNA残留,因此第二步利用环状DNA耐受限制性外切酶的特点,用外切酶对柱纯化后产物进行酶消化。对人类样品,会特别的先使用针对人类线粒体的限制性内切酶MssI将环状的线粒体DNA剪切成线性DNA,再进行外切酶消化,一并去除线粒体DNA。

3)滚环扩增
经过前两步酶消化和纯化,基因组线性DNA被去除,保留下来的环状DNA因为总量较少,所以需要通过滚环扩增放大环状DNA信号,使之达到建库所需的DNA量。

4)建库测序
对纯化和扩增富集的后的环状DNA,进行常规的NGS高通量测序。流程包括片段化,建库和使用Illunina NovaSeq测序仪进行150bp双端测序。

技术优势:
- 使用原装A&A biotechnology纯化柱高效富集环状DNA
- 滚环扩增放大环状DNA信号,提高检出率
- 专业的生信分析:详尽的注释、丰富的图表
2.血清血浆环状DNA测序
针对血清血浆微量样品,云序生物参考卢煜明教授团队开发的方法,酶切去除线性DNA后,利用Tn5转座酶,打开eccDNA环状结构并同时在DN**段两端加上接头,进行建库及测序。Tn5转座酶法效率高,损耗低,实现血液循环系统中微量的环状DNA的检测。并且本产品能保留环状DNA的原始表达量,使得不同环状DNA间的表达量的比较更为准确。
参考文献:
Identification and characterization of extrachromosomal circular DNA in maternal plasma
实验流程:
1)环状DNA富集:通过核酸外切酶 V 消化等手段,去除样品中的线性DNA,从而达到富集环状DNA的目的。
2)加接头:通过转座酶打开环状DNA的环形结构,并在DN**段的两端加上接头。
3)末端修复:通过Klenow酶修复转座产物的末端缺口。
4)建库测序:纯化后文库质检合格后进行上机测序。
技术优势:
- 减少DNA损失
- 保留原始表达量,不同环状DNA间表达量比较更准确
3.血清血浆环状DNA甲基化测序
针对血清血浆样品,云序参考卢煜明教授团队今年研发的方法,酶切去除线性DNA后,利用Tn5转座酶,打开环状DNA环状结构并同时在DN**段两端加上接头,并用酶转化法将未甲基化的C转化为U,进行建库及测序。一次建库测序中同时检测样品中环状DNA及其甲基化位点的信息。
参考文献:
Characteristics of Fetal Extrachromosomal Circular DNA in Maternal Plasma: Methylation Status and Clearance
实验流程:
1)环状DNA富集:通过核酸外切酶 V 消化等手段,去除样品中的线性DNA,从而达到富集环状DNA的目的。
2)加接头:通过转座酶打开环状DNA的环形结构,并在DN**段的两端加上接头。
3)末端修复:通过Klenow酶修复转座产物的末端缺口。
4)C-U转化:通过温和的酶转化法,将未甲基化的胞嘧啶(C)高效地转化为尿嘧啶(U)。
5)PCR扩增:对转化后产物进行PCR扩增及纯化。
6)上机测序:纯化后文库质检合格后进行上机测序。
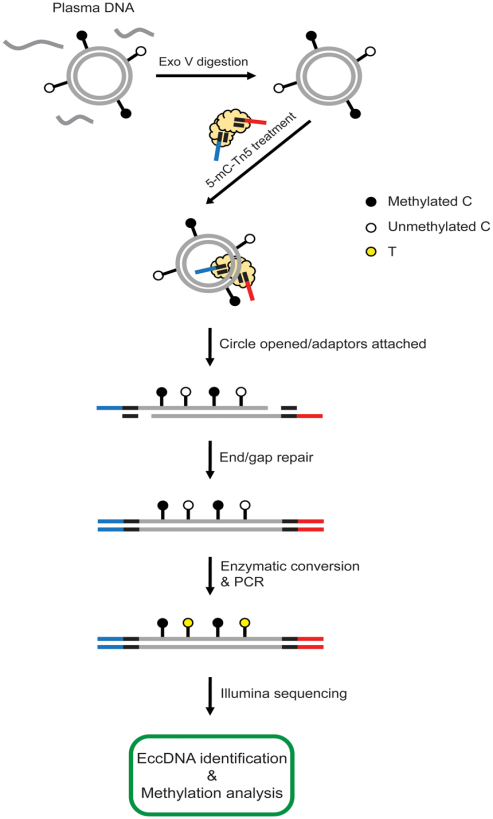
技术优势:
- 一箭双雕:同时检测环状DNA及其甲基化状况,节约样品,性价比高
- 单碱基分辨的环状DNA甲基化分析
4.环状DNA sanger测序
针对测序项目中筛选出的环状DNA,云序提供sanger测序服务验证环状结构。其主要目的在于:为用户提供一种低成本的扩大样品量验证手段,节约实验成本。通过设计反向引物进行PCR扩增,将覆盖环状DNA连接位点的扩增产物进行sanger测序,验证连接位点处序列。
原理:
针对环状DNA的break point设计反向引物
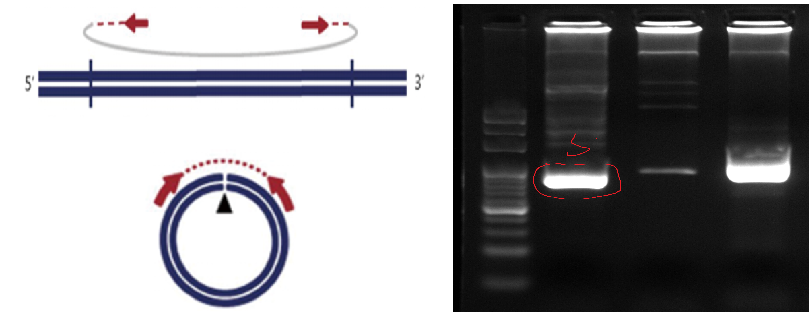
结果展示:
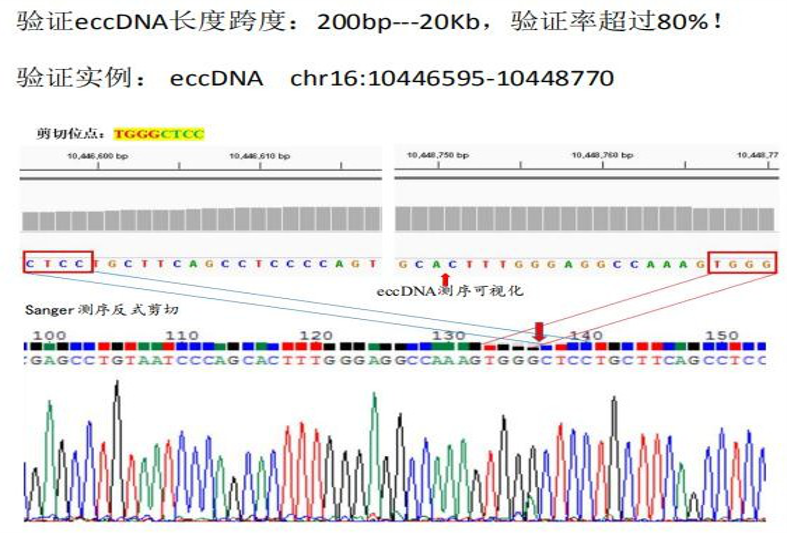
5.环状DNA纯化柱
A&A Biotechnology的纯化柱,是绝大部分环状DNA高分文章中所使用的纯化柱。云序生物是该品牌在国内的唯yi总代理。

ATAC-Seq
ChIP-Seq
Cut&Tag
MeDIP-Seq
hMeDIP-seq
外显子组测序
全基因组测序
往期环状DNA主题回顾
了解更多环状DNA相关主题文章,可关注“云序生物课堂”微信公众号:
NIPT之父卢煜明揭秘染色体外环状DNA甲基化
全国首fa!云序再推eccDNA重磅新品:eccDNA甲基化测序
Cancer Cell研究新进展:eccDNA调控癌基因转录
斯坦福大学新研究----肿瘤细胞中ecDNA新机制
Nature重磅新星——eccDNA的物种发现史
2020国自然研究热点—eccDNA的前世今生
eccDNA新型生物标志物,卢煜明团队zui新重磅成果!
再登Nature Genetics:ecDNA与致癌基因扩增及多种癌症不良预后相关
10分文章新利器----eccDNA开启2020年科研新热点
颠覆性发现:癌基因竟不在染色体上 环状DNA连登Nature,Cell!
Nature Genetics 揭示eccDNA新功能—驱动神经母细胞瘤基因组重排
